در این مطلب نمونه سوال امتحانی شیمی دهم برای شما دانش آموزان گرامی قرار داده شده است.
کتاب شیمی دهم سه فصل دارد:
- فصل اول – کیهان، زادگاه الفبای هستی
- فصل دوم – ردپای گازها در زندگی
- فصل سوم – آب، آهنگ زندگی
تقسیم بندی مباحث و بارم بندی شیمی دهم در امتحانات نوبت اول، نوبت دوم و شهریورماه به صورت زیر می باشد:
بارم بندی امتحانات نوبت اول (دی ماه):
- فصل اول:کیهان، زادگاه الفبای هستی – 12 نمره
- فصل دوم: ردپای گازها در زندگی (تا صفحه 64) – 8 نمره
بارم بندی امتحانات نوبت دوم (خردادماه):
- فصل اول:کیهان، زادگاه الفبای هستی – 5 نمره
- فصل دوم: ردپای گازها در زندگی (تا صفحه 64) – 2 نمره
- فصل دوم: ردپای گازها در زندگی (از صفحه 6 تا پایان فصل) – 5 نمره
- فصل سوم: آب، آهنگ زندگی – 8 نمره
نمونه سوال امتحانی شیمی دهم نوبت اول
کتاب شیمی دهم از 3 فصل تشکیل شده است . شیمی دهم برای رشته های ریاضی و تجربی مشترک است .
فصل اول کتاب شیمی دهم :کیهان زادگاه الفبای هستی
فصل دوم کتاب شیمی دهم :رد پای گازها در زندگی
فصل سوم کتاب شیمی دهم :آب آهنگ زندگی
نمونه سوال امتحانی شیمی دهم نوبت دوم
در فصل اول ((کیهان زادگاه الفبای هستی)) با عناوین زیر بررسی می گردد:
عنصرها چگونه پدید آمدند؟
رابطه انیشتین :
درون ستاره به دلیل انجام واکنش های هسته ای،انرژی بسیار زیادی آزاد می شود.انیشتین رابطه زیر را برای محاسبه ی انرژی تولید شده در این واکنش ها ارایه کرد :

ایزوتوپ :
ایزوتوپ های یک عنصر عدد اتمی(z) یکسان و عدد جرمی(A) متفاوت دارند که تفاوت در عدد جرمی ناشی از تفاوت در تعداد نوترون ها است .
تکنسیم،نخستین عنصر ساخت بشر:
تکنسیم نخستین عنصری بود که در واکنشگاه (راکتور هسته ای) ساخته شد،این رادیوایزوتوپ در تصویربرداری پزشکی کاربرد ویژه ای دارد.از این عنصر برای تصویر برداری غده ی تیروئید استفاده می شود.
جدول دوره ای عناصر
در جدول دوره ای (تناوبی)امروزی،عنصر ها براساس افزایش عدد اتمی ساماندهی شده اند.
جرم اتمی عنصرها
اتم ها بسیار ریز هستند به طوری که نمی توان آن ها را به طور مستقیم مشاهده و جرم آن ها را اندازه گیری کرد.
به همین دلیل دانشمندان مقیاس جرم نسبی را برای تعیین جرم اتم ها به کار می برند.
نور کلید شناخت جهان
نور خورشید اگرچه سفید به نظر می رسد ولی گستره ی رنگی شامل بی نهایت طول موج از رنگ های گوناگون است .
نشر نور و طیف نشری
عنصر ها ی مختلف وقتی روی شعله قرار می گیرند،رنگ شعله تغییر می کند.برای نمونه رنگ شعله فلز سدیم و ترکیب های گوناگون آن مشابه و زرد رنگ است .
رنگ شعله فلز لیتیم و ترکیب های گوناگون آن مشابه و سرخ است .
عدد کوانتومی اصلی (n)
عددی است که مشخص می کند الکترون در کدام سطح انرژی اصلی قرار گرفته است .
عدد کوانتومی فرعی
هر لایه الکترونی از بخش های کوچک تری به نام زیر لایه تشکیل شده است.
آرایش الکترونی اتم
قاعده آفبا ترتیب پر شدن زیرلایه ها را در اتم های گوناگون نشان می دهند که طبق آن ترتیب پر شدن به این صورت است :
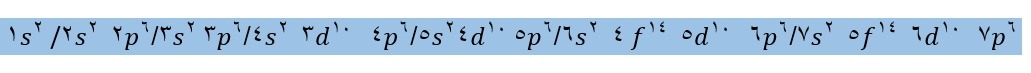
ساختار اتم و رفتار آن
بین پایداری و آرایش الکترونی لایه ظرفیت اتم ها رابطه ای وجود دارد.به طوری که اگر لایه ظرفیت اتمی هشت تایی باشد،آن اتم واکنش پذیری چندانی ندارد.
لوویس برای توضیح رفتار اتم ها آرایش الکترون_ نقطه ای ارائه کرد که در آن الکترون های ظرفیت هر اتم پیرامون نماد شیمیایی آن با نقطه نمایش داده می شود.
گازهای نجیب در بیرونی ترین لایه الککترونی خود دارای هشت الکترون هستند که آرایش الکترونی آن ها به صورت زیر نمایش داده می شود که این آرایش پایدار است .
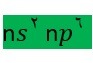
تبدیل اتم ها به یون ها
ترکیب یونی ترکیبی است که ذرات سازنده آن یون هستند.هر ترکیب یونی از لحاظ بار الکتریکی خنثی است زیرا مجموع بار الکتریکی کاتیون ها با مجموع بار الکتریکی آنیون ها برابر است .
تبدیل اتم ها به مولکول ها
پیوند کوالانسی (اشتراکی ) پیوندی است که در آن اتم ها برای رسیدن به حالت پایدار خود به تعداد برابر الکترون به اشتراک می گذارند.

در فصل دوم (( رد پای گازها در زندگی )) سر فصل های زیر بررسی می شود :
هوا کره : لایه فیروزه ای پیرامون زمین ،اتمسفر زمین یا همان هوا کره است که اغلب هوا نامیده می شود.
هوا کره لایه لایه است و هر لایه ویژگی های متفاوتی دارد که دما و فشار هوا کره از جمله عوامل مهم در تعیین ویژگی هاست.
|
با افزایش ارتفاع از سطح زمین ،فشار و چگالی هوا کمتر می شود. |
آرگون :گاز نجیب بی رنگ،بی بو و غیر سمی است.آرگون به عنوان محیط بی اثر در جوشکاری،برش فلزها و در ساخت لامپ های رشته ای،به کار می رود.
هلیم : سبک ترین گاز نجیب است.گازی بی رنگ و بی بو. هلیم در کره زمین به مقدار خیلی کم یافت می شود و مقدار بیشتری از این گاز در لایه های زیرین پوسته زمین وجود دارد.
از هلیم برای پر کردن بالن های هواشناسی،تفریحی و تبلیغاتی در جوشکاری،کپسول غواصی و مهم تر از همه برای خنک کردن قطعات الکترونیکی دردستگاه های تصویر برداری مانند MRI استفاده می شود.
اکسیژن : اکسیژن از مهم ترین گازهای تشکیل دهنده هوا کره است که زندگی روی زمین به وجود آن گره خورده است .
این عنصر در آب کره(ساختار مولکول های آب )سنگ کره ( به صورت ترکیب با دیگر عنصر ها ) و در هوا کره به طور عمده به شکل مولکول های دو اتمی O2 وجوددارد.
اکسیژن گازی واکنش پذیر است و با اغلب عنصر ها و مواد واکنش می دهد.
کربن مونوکسید:
گازی بی رنگ ،بی بو و بسیار سمی است .چگالی این گاز کمتر از هوا است و قابلیت انتشار آن در محیط بسیار زیاد است.
به طوری که به سرعت در همه فضای اتاق پخش میشود.
از آن جا که میل ترکیبی هموگلوبین خون با این گاز بسیار زیاد و بیش از 200 برابر اکسیژن است ،مولکول های آن پس از اتصال به هموگلوبین از رسیدن به بافت های بدن
جلوگیری می کنند.
این ویژگی باعث مسمومیت می شود و سیستم عصبی را فلج می کند و قدرت هر اقدامی از فرد را می گیرد و باعث مرگ وی می شود.
به طوری که به سرعت در همه فضای اتاق پخش می شود.از آن جا که میل ترکیبی هموگلوبین خون با این گاز بسیار زیاد و بیش از 200 برابر
اکسیژن است،مولکول های آن پس از اتصال به هموگلوبین از رسیدن اکسیژن به بافت های بدن جلوگیری می کنند.
این ویژگی باعث مسمومیت می شود،سامانه عصبی را فلج می کند و قدرت هر اقدامی را از فرد می گیرد و باعث مرگ می شود.
ترکیب اکسیژن با فلز هاو نا فلز ها :
فلز ها و دستگاه های فلزی وقتی در معرض هوا قرار می گیرند،دچار تغییرشیمیایی شده و دوباره با اکسیژن هوا ترکیب می شوند.
برای مثال واکنش زنگ زدن آهن واکنش اکسایشی است که در آن آهن با اکسیژن در هوای مرطوب واکنش داده و زنگ آهن قهوه ای تشکیل می دهد.
به واکنش آرام مواد با اکسیژن که با تولید انرژی همراه است ،اکسایش میگویند.
نام گذاری ترکیبات یونی و مولکولی
یون های تک اتمی که ظرفیت متغیر دارند، داخل پرانتز بار یون با عدد رومی نشان داده می شود.
اگر یونی ظرفیت ثابت داشته باشد هرگز از عددهای رومی استفاده نمی کنیم.
یون هایی که ظرفیت متغیر دارند همگی کاتیون هستند.
اگر در فرمول مولکولی یک ترکیب،تنها یک اتم از عنصر سمت چپ وجود داشته باشد،از پیشوند مونو پیش از نام آن استفاده نمی کنیم.
****ساختار لوویس***
قواعد رسم ساختار لوویس به این صورت است :
1-ابتدا اتم مرکزی را مشخص می کنیم و مدل الکترون _نقطه ای آن را رسم می کنیم.
2-اتم های اطراف را پیرامون اتم مرکزی قرار می دهیم و مدل الکترون _نقطه ای آن ها را براساس تعداد الکترون های لایه ظرفیت رسم می کنیم.
3-الکترون های منفرد اتم های پیرامون را به الکترون های منفرد اتم مرکزی وصل می کنیم.
**نکته : الکترون های ناپیوندی روی اتم ها را با جفت نقطه نمایش می دهیم.
بعد از رسم ساختار لوویس پیرامون هر اتم در مجموع هشت الکترون (پیوندی +نا پیوندی )وجود دارد.
هر جفت الکترون پیوندی را با یک خط نمایش می دهیم.اگر میان دو اتم دو جفت الکترون پیوندی باشد،با دو خط و اگر سه جفت الکترون پیوندی باشد
با سه خط نمایش می دهیم .
خواص اکسید های فلزی و نافلزی :
به طور کلی اکسیدهای فلزی را اکسید بازی و اکسید های نا فلزی را اکسید های اسیدی می نامند؛زیرا از واکنش آن ها با آب به ترتیب باز و اسید تولید می شود.
باران اسیدی چیست : باران به دلیل وجود کربن دی اکسید محلول در آن اندکی اسدی است و PH کمتر از 7 دارد.
اما آلاینده های موجود در هوا که بر اثر فعالیت های انسانی به هواکره وارد شده اند و در آب حل شده و به آن خاصیت اسیدی چشمگیری می بخشند .
اوزون O2: دگر شکلی از اکسیژن و گازی با مولکول های سه اتمی در لایه های بالایی هواکره(استراتوسفر) بوده که مانند پوششی کره زمین را احاطه کرده است
و مانع از رسیدن پرتوهای پر انرژی و زیان آور فرابنفش به سطح زمین می رسد.
اوزون تروپوسفری از کجا می آید؟
گاز نیتروژن به عنوان اصلی ترین جزء سازنده هوا کره واکنش پذیری بسیار کمی دارد و به طور معمول با اکسیژن واکنش نمی دهد.
اما هنگام رعد و برق این دو گاز در هوا ترکیب شده و به اکسیدهای نیتروژن تبدیل می شوند.
تولید آمونیاک
گاز نیتروژن فراوان ترین جزء سازنده هواکره در مقایسه با اکسیژن از نظرشیمیایی غیرفعال و واکنش پذیر است .
مخلوطی از گازهای اکسیژن در حضور کاتالیزگر یاجرقه در یک واکنش سریع و شدید منفجر شده و آب تولید می کند اما در مخلوطی از گاز نیتروژن و هیدروژن
در حضور کاتالیزگر یاجرقه هیچ واکنشی رخ نمی دهد.
درفصل سوم (آب آهنگ زندگی ) با عناوین زیر آشنا می شویم :
آب وهمراهان نا پیدای آن
نزدیک به 75 درصد سطح زمین را آب پوشانده است.
آب اقیانوس ها و دریاها مخلوطی همگن است که اغلب مزه ای شور دارد؛زیرا مقدار قابل توجهی از نمک های گوناگون در آن حل شده است .
کره زمین را می توان سامانه بزرگی در نظر گرفت که شامل 4 بخش هواکره ، آب کره و سنگ کره وزیست کره می باشد .
یون فلوئورید
به آب آشامیدنی مقدار بسیار کمی یون فلوئورید می افزایند؛زیرا این یون باعث حفظ سلامت دندان ها می شود.
محلول و مقدار حل شونده ها
محلول،مخلوطی همگن از دو یا چند ماده است که حالت فیزیکی و ترکیب شیمیایی محلول در سر تا سر آن یکسان و یکنواخت است.
.هوای پاکی که تنفس می کنیم محلولی از گاز هاست .
سرم فیزیولوژی محلول نمک در آب است .
ضد یخ محلول اتیلن گلیکول در آب است .گلاب مخلوطی همگن از چند ماده آلی در آب است .
در ارتباط با مباحث و مسائل محلول ها موارد زیر بررسی می شود:

انحلال پذیری
*واژه بیشترین نشان دهنده رسیدن محلول به حالت سیر شده است.
*نمک های گرماگیر با افزایش دما،انحلال پذیریشان افزایش می یابدو نمک های گرماده با افزایش دما،انحلال پذیرشان کاهش میابد.
انواع محلول ها
1-سیر شده:محلولی که حداکثر مقدار ماده حل شونده را در خود حل کرده است.
2-محلول سیر نشده :محلولی که هنوز می تواند مقدار ماده حل شونده بیشتری را در خود حل کند.
3-محلول فرا سیر شده:محلولی که ابتدا در دمای بالاتر سیر شده است ،آرام آرام سرد کنیم.
رفتار آب ودیگر مولکول ها در میدان الکتریکی
آب ویژگی گوناگونی دارد؛از جمله توانایی حل کردن اغلب مواد،افزایش حجم هنگام انجماد و داشتن نقطه ی جوش بالا و غیرعادی است.
شکل مولکول آب خمیده (V شکل) است .
نیروهای بین مولکولی آب
به بر هم کنش میان مولکول های سازنده ی یک ماده نیوهای بین مولکولی می گویند.گازها مولکول های مجزا دارند،بنابراین کمترین بر هم کنش ها را دارند،اما در مایع ها بر هم کنش مولکول ها بیشتر است و در جامدها برهم کنش میان مولکول ها می تواند به بیشترین مقدار ممکن برسد.
آب و دیگر حلال ها
*برخی موادشیمیایی مانند اتانول(الکل معمولی ) و استون به هر نسبتی در آب حل می شوند .
*آب و استون گشتاور دو قطبی بالایی دارند و به هر نسبتی در یکدیگر حل می شوند.
*ید و هگزان گشتاور دو قطبی صفر دارند،بنا براین ناقطبی هستند؛پس شبیه بهم بوده و در هم حل می شوند.
تفکیک یونی در فرآیند انحلال
در انحلال مولکولی مولکول های حل شونده ماهیت خود را ر محلول حفظ میکنند،گویی ساختار مولکول های حل شونده در محلول دچار تغییر نشده است .
انحلال گازها
انحلال پذیری گاز ها در آب به دما،فشار و نوع گاز وابسته است .
الف)با افزایش دما،انحلال پذیری گاز ها در آب کاهش می یابد.
ب)با افزایش فشار،انحلال پذیری گازها در آب افزایش می باید .
ج)انحلال پذیری گازها در آب به نوع گاز وابسته است.هرچه گاز قطبی تر باشد ،نیروی جاذبه قوی تری با آب ایجاد می کند وانحلال پذیری بیشتر می شود.
رسانایی الکتریکی محلول ها
فلزها و گرافیت (مغز مداد) رسانای جریان برق هستند و چون الکترون آزاد دارند ،به آن ها رسانای الکترونی می گویند.
نوع دیگری از رسانایی وجود دارد که به وسیله ی یون ها انجام میشود و به آن رسانای یونی می گویند.
در این نوع رسانایی یون ها می توانند از یک نقطه به نقطه دیگر جابه جا شوند زیرا در این شرایط بارهای الکتریکی هم جابه جا خواهند شد.
اسمز
دیواره یاخته ها در گیاهان روزنه هایی بسیار ریز دارد که ذره های سازنده مواد می توانند از آن عبور کنند.
به گونه ای که این روزنه ها فقط اجازه عبور به برخی از ذره ها و مولکول های کوچک مانند آب و یون ها را می دهند و از عبور مولکول های درشت تر
جلوگیری می کنند.این دیواره ها غشای نیمه تراوا نامیده می شوند.
بااین روش می توان آب دریا را نمک زدایی و آب شیرین تهیه کرد؛زیرا یون ها به وسیله غشای نیمه تراوا از مولکول های آب جدا می شوند.
این فرآیند را اسمز وارونه می نامند.
زیرا در جهت وارون با اعمال فشار از غشای نیمه تراوا به عقب رانده می شوند.



